生物制品生产工艺介绍

引言
生物制品是指利用生物技术,通过细胞、微生物、生物组织等生物体或其组成部分生产出的用于预防、诊断和治疗人类疾病的药品,如疫苗、抗体、重组蛋白、基因治疗产品等。其生产工艺与传统化学合成药物有显著区别,具有高度复杂性、精密性和对生产环境与条件的严苛要求。本课件旨在系统介绍生物制品生产的主要工艺流程、关键技术环节和质量控制要点。
一、 核心工艺路线概述
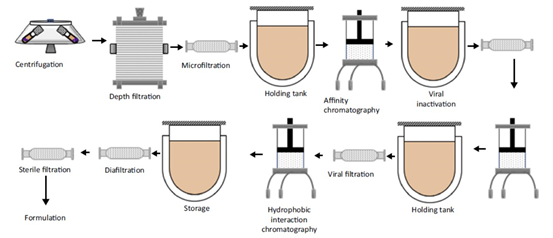
生物制品的典型生产工艺遵循一条主线:构建 → 培养 → 纯化 → 制剂 → 包装。
- 上游工艺:细胞培养与表达
- 细胞系/菌种构建:这是生产的起点。通过基因工程技术,将编码目标蛋白(如抗体)的基因导入合适的宿主细胞(如中国仓鼠卵巢细胞CHO、大肠杆菌、酵母等),筛选出能稳定、高效表达目标产物的细胞株或工程菌株。
- 细胞扩增与发酵:将筛选出的“种子细胞”在严格控制的生物反应器中逐级放大培养。过程需精确控制温度、pH、溶氧、营养物质(培养基)等参数,以最大化细胞生长和目标产物的产量。
- 下游工艺:分离与纯化
- 此阶段目标是将目标产物从复杂的培养液中高效分离出来,并去除杂质(如宿主细胞蛋白、DNA、内毒素、培养基成分等)。
- 收获与澄清:通过离心、过滤等方法去除细胞或细胞碎片,获得澄清的含有目标产物的料液。
- 捕获(初步纯化):常采用亲和层析(如Protein A层析纯化抗体)高效、特异地捕获目标产物,实现初步浓缩和纯化。
- 精纯(中度与深度纯化):利用离子交换层析、疏水层析、分子筛层析等多种层析技术,进一步去除各类杂质,使产品纯度达到极高标准(通常>99%)。
- 病毒去除/灭活:对于哺乳动物细胞生产的制品,这是关键安全步骤。采用低pH孵育、溶剂/去污剂处理、纳米过滤等已验证的方法,确保灭活或去除潜在的外源病毒。
- 制剂与灌装
- 制剂:将高纯度的原液配制成适合临床使用的最终剂型。需添加稳定剂、缓冲液等赋形剂,并调整至适宜的浓度和pH,确保产品在储存期间的稳定性、安全性和有效性。
- 无菌灌装与冻干:在A级洁净环境下,将制剂灌装到西林瓶或预充针中。部分对热敏感的产品需要进行冷冻干燥(冻干),以形成固体状态,延长保存期限。
二、 关键技术与系统支持
- 细胞培养技术:包括贴壁培养、悬浮培养、灌流培养、高密度发酵等,直接影响产量和成本。
- 层析纯化技术:是下游工艺的核心,其分离效率和选择性决定了产品的纯度和收率。
- 过程分析技术(PAT):通过在线、实时监测关键工艺参数,实现对生产过程的动态控制,确保工艺稳定和产品质量一致。
- 一次性技术:使用一次性生物反应袋、储液袋、管路和连接器,可减少交叉污染风险、缩短清洁验证时间、提高生产灵活性,在现代生物制品生产中应用广泛。
- 自动化与信息化:采用分布式控制系统(DCS)或可编程逻辑控制器(PLC)实现自动化生产,并通过制造执行系统(MES)管理生产流程和数据,确保合规性与可追溯性。
三、 质量控制与法规符合性
生物制品的生产必须全程遵循 药品生产质量管理规范(GMP)。质量控制贯穿始终:
- 原材料控制:对细胞库、培养基、血清、化学品等所有物料进行严格检定和管理。
- 过程控制:对每个工艺步骤的关键参数和中间产物进行在线或离线检测。
- 放行检测:成品必须经过全面的质量检验,包括鉴别、纯度、效价、含量、安全性(无菌、内毒素、宿主残留、外源病毒等) 等项目,全部合格后方可放行。
- 持续工艺验证:确保生产工艺能持续稳定地生产出符合预定标准的产品。
四、 发展趋势与挑战
- 连续生产工艺:相比传统的批次生产,连续生产可提高设备利用率、缩小生产规模、提高产品一致性,是未来的重要发展方向。
- 个性化与先进疗法:如CAR-T细胞治疗等个体化产品,其生产工艺更需灵活、快速和高度定制化。
- 成本控制:生物制品生产成本高昂,通过提高细胞表达量、优化纯化工艺、应用一次性技术等是降低成本的焦点。
- 质量源于设计(QbD):在工艺开发初期就系统地研究产品、工艺与质量属性之间的关系,建立科学的设计空间,实现更稳健的生产。
###
生物制品的生产工艺是一个集生物学、工程学、化学和信息学于一体的复杂系统工程。其成功依赖于稳定可靠的细胞系、精密优化的工艺流程、严格的过程控制以及全方位的质量管理体系。随着技术的不断进步,生物制品的生产工艺正朝着更高效、更灵活、更智能和更经济的方向发展,以满足日益增长的临床需求。
如若转载,请注明出处:http://www.shulindaifangxihu.com/product/66.html
更新时间:2026-02-27 20:13:52